2.1 纳入文献的基本情况 共纳入32篇文献,其中23篇涉及有关诱导性多潜能干细胞诱导方法、筛选鉴定、诱导效率和安全性的研究,4篇涉及诱导性多潜能干细胞在建立疾病模型方面的研究,5篇涉及诱导性多潜能干细胞应用于疾病治疗的研究。
2.2 结果
2.2.1 诱导性多潜能干细胞的建立
诱导性多潜能干细胞的诱导方法及诱导效率:通过导入特定的转录因子可将成体细胞重编程为诱导性多能干细胞,最初研究者们应用反转录病毒为载体将转录因子导入成体细胞,但由于此种方法可能使外源基因插入细胞的基因组中引起插入突变,故存在一定的安全隐患;另外,转染效率低也是诱导性多潜能干细胞技术的一个主要障碍,于是研究者们开始探寻一些可以避免基因插入突变并且能够提高诱导效率的新方法。
不同诱导方法及诱导剂的探索:Stadtfeld等[2]发现,利用小鼠成纤维细胞,只需含有一个拷贝的Oct4转基因成分,就能通过腺病毒载体将Sox2、c-Myc和Klf4这3个基因转入小鼠成纤维细胞而成功诱导出诱导性多潜能干细胞。Okita等[3]研究者则使用质粒来转染细胞。他们使用2个质粒,一个质粒携带Oct4、Klf4和Sox2基因,而另一个质粒携带c-Myc基因,重复转染小鼠胚胎成纤维细胞7 d后成功诱导出诱导性多潜能干细胞。但和使用腺病毒载体一样,质粒载体的效率相比反转录病毒载体来说更低。并且使用质粒载体也可能出现外源基因随机整合入细胞基因组的情况。
随着诱导性多潜能干细胞重编程方法的不断探索,研究者们发现了另一种避免细胞基因组插入突变的办法就是使用小分子物质来替代细胞重编程过程中使用的外源基因,这些小分子物质还能提高转染效率,2009年10月,美国Scripps研究所丁盛博士等发现,在培养液中加入一些小分子化合物如SB43142和PD0325901时,可以显著提高重编程的效率[4]。Huang等[5]在研究中发现只转染2个因子Oct4和Sox2,再加上丙戊酸(valproic acid, VPA),就能将人类成纤维细胞重编程为诱导性多潜能干细胞。现在人们通过试验发现在人类和小鼠细胞试验中,VPA都可以很大地提高重编程的效率。还有研究者发现在培养过程中添加维生素C可提高iPS重编程效率,它可促进基因表达从而加速体细胞进入重编程状态[6]。
由于mRNA、miRNA及siRNA具有不会插入哺乳动物基因组的特点,所以在诱导诱导性多潜能干细胞中有着独特的优势。Warren等[7]将Oct4、Sox2、Klf4、c-Myc这4个关键蛋白质的mRNA导入人皮肤细胞,得到核糖核酸诱导多能干细胞,使细胞重编程的速度提高了1倍,而重编程效率是标准方法的100倍以上,并且没有发生基因组结构改变,核糖核酸诱导多能干细胞比一般的诱导性多潜能干细胞更具备胚胎干细胞的特点。与此同时,有研究用miRNA诱导小鼠和人体细胞生成了诱导性多潜能干细胞,也将重编程效率提高了将近100倍。通过在小鼠胚胎成纤维细胞中表达miR302/367的miRNA簇而获得了类似于诱导性多潜能干细胞的群落,分析其原因,认为可能与其能激活Oct4并抑制HDAC2(组蛋白脱乙酰基酶)的活性有关[8]。
p53是调控细胞程序重排的关键因子,Hong等[9]发现去除c-Myc基因后用siRNA阻断p53基因的路径,可以将皮肤细胞转化为诱导性多潜能干细胞的成功率提高至10%左右,也有研究证明,p53对诱导性多潜能干细胞的转化效率起重要的作用。
不同组织来源细胞诱导为诱导性多潜能干细胞的效率比较:不同组织来源的细胞诱导生成诱导性多潜能干细胞的效率也是不相同的[10],见表1。
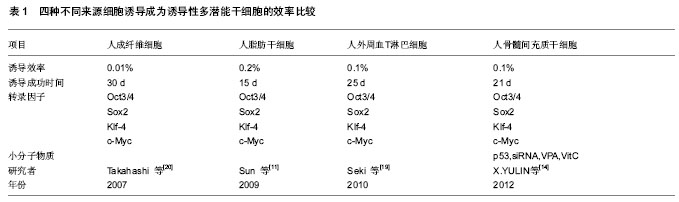
2009年,斯坦福大学研究者Sun等[11]发现,人脂肪干细胞比人皮肤成纤维细胞更容易被诱导为诱导性多潜能干细胞,其诱导效率为0.2%,是人皮肤成纤维细胞的20倍。
Aasen等[12]用从发根鞘部位生发的角质层表皮干样细胞,通过反转录病毒介导表达Oct-4、Sox2、Klf4及c-Myc也成功诱导生成了诱导性多潜能干细胞,且经过mRNA水平检测,发现其诱导效率与成纤维细胞相比大约提高了100倍,而且诱导多潜能干细胞克隆出现的时间也缩短至10 d。
之后由Ruiz等[13]研究发现利用星形胶质细胞诱导成为诱导性多潜能干细胞,其诱导效率与胶质层表皮样干细胞相当。
2012年,浙江大学医学院Yulin等[14]研究者在应用人骨髓间充质干细胞诱导生成诱导性多潜能干细胞时发现,使用p53siRNA、VPA、维生素C和4个转录因子共同参与诱导性多潜能干细胞重编程过程时,前三者具有协同作用,并且这些物质的组合使用可以通过抑制p53基因的表达、缩减细胞凋亡,上调多能性基因Oct4的表达并修饰细胞周期而显著提高了诱导性多潜能干细胞的生成效率。
此外,外周血采集方便、来源丰富,可缩短诱导性多潜能干细胞的诱导成功时间,且经研究发现其诱导效率可以达到0.1%,是成纤维细胞的10倍,与成纤维细胞和内皮细胞相比,人外周血单个核细胞和CD43+细胞基因组启动子甲基化水平更接近胚胎干细胞和诱导性多潜能干细胞[15]。
Kim等[16]的研究结果指出,小鼠血细胞重编程的诱导性多潜能干细胞与成纤维细胞诱导性多潜能干细胞相比更具有类似于胚胎干细胞的形态与功能。
2010年,Cell Stem Cell同时报导了3个研究小组重编程人外周血细胞获得诱导性多潜能干细胞的工作,外周血重编程研究取得了重大突破[17-19]。
诱导性多潜能干细胞的筛选和鉴定:Takahash和Yamanaka[1]实验小组采用体外基因转染技术将24种转录因子排列组合导入小鼠成纤维细胞,最终筛选出了Oct4、Sox2、c-Myc、Klf4这4个因子,以反转录病毒为载体,以Fbx15为筛选标志(Fbx15是细胞多能性的一个标志分子),利用同源重组技术将融合的β半乳糖苷酶基因和新霉素抗性基因(neo)整合到Fbx15基因位点,利用这几个基因激活内源性Fbx15-neo表现的G418抗性来筛选诱导性多潜能干细胞,用这种方法得到的克隆细胞称为Fbx15+诱导性多潜能干细胞。这样得到的诱导性多潜能干细胞能形成畸胎瘤和嵌合体小鼠胚胎,但是不能形成成年嵌合体小鼠,也没有生殖系转移的能力,Fbx5+iPS具有胚胎干细胞的部分特征,但是其基因表达水平和甲基化模式则与胚胎干细胞有所不同,造成这种差别的主要原因是使用了Fbx15启动子表达的新霉素抗性基因作为筛选标志,尽管Fbx15在未分化的胚胎干细胞中表达量较高,但Fbx15在胚胎干细胞的自我更新和多潜能性的维持中不是必须的。
2007年,Okita等[3],通过同源重组的方法将新霉素抗性基因整合到对细胞多能性更加关键的基因(Oct4和Nanog)位点,并筛选出了稳定的诱导性多潜能干细胞系(Oct4+iPSCs和Nanog+iPSCs),并比较了两者的筛选效果,发现Oct4+iPS的诱导效率较高,是Nanog+iPSCs的10倍,但是Nanog位点比较容易激活。与Fbx15筛选相比,Nanog+iPSCs具有更多胚胎干细胞特征。
筛选过程中时间的选择也很重要,细胞重编程是一个缓慢渐进的过程,随着时间的延长,多能性基因逐渐激活,得到的抗性细胞在数量上会有所增加。且经Takahash,Yamanaka等[1]实验验证,低氧浓度(体积分数5%的氧)对于诱导性多潜能干细胞的培养是比较适宜的。
诱导性多潜能干细胞经过筛选后,需要进行生物学特性鉴定,目前,研究人员主要通过形态学标准、标志分子的表达、表观遗传状态、基因表达模式和发育潜能等方面对诱导性多潜能干细胞其进行鉴定。主要通过以下几个方面进行:①细胞形态学观察与AP染色:生长在饲养层上的人诱导性多潜能干细胞呈典型的克隆状生长。克隆呈圆形或椭圆形,边界清晰;克隆内细胞排列紧密,细胞体积小、核大、细胞核/质比高,AP染色呈阳性。②利用免疫荧光检测胚胎干细胞标志性抗原的表达:包括TRA-1-81,TRA-1-60,SSEA4,Nanog和SSEA3等。③提取诱导性多潜能干细胞总RNA,qRT-PCR检测胚胎干细胞内源性多功能基因及转基因表达情况:内源性多功能基因包括Oct4,Sox2,Nanog,Lin28,Sall4,Nodal,Dppa2,TERT,TDGF1,DPPA4等。④诱导性多潜能干细胞染色体核型分析。⑤悬浮培养观察拟胚体形成及体外分化情况。⑥诱导性多潜能干细胞接种至SCID小鼠皮下,观察畸胎瘤形成及体内分化情况。
2.2.2 诱导性多潜能干细胞的多能性及全能性 诱导性多潜能干细胞与胚胎干细胞有着相似的特性,其中一个最重要的特性就是具有强大的自我更新能力以及多向分化潜能且具备全能性。诱导性多潜能干细胞具有与胚胎干细胞类似的形态和生长特性,同时也表达胚胎干细胞的特异性标记;实验证实将细胞移植入裸鼠皮下,可以生长出3种不同胚层来源的畸胎瘤,这表明诱导性多潜能干细胞具有多分化潜能;研究者通过亚硫酸盐基因组测序法、萤光素酶报告基因实验、染色质免疫沉淀技术(chromatin immunoprecitation,CHIP)技术,发现了诱导性多潜能干细胞与胚胎干细胞具有相似的DNA甲基化模式和组蛋白修饰情况。
然而检测诱导性多潜能干细胞是否具有全能性的最高标准就是验证该细胞是否能够培育出完整的小鼠。2009年7月23日,中科院动物研究所周琪研究员和上海交通大学曾凡一研究员及其实验小组,分别采用反转录病毒和慢病毒转染的方法,首次利用诱导性多潜能干细胞,通过四倍体囊胚注射得到存活并具有繁殖能力的小鼠—“小小”,从而首次在世界上证明了诱导性多潜能干细胞全能性[21]。
2.2.3 诱导性多潜能干细胞的安全性 由于诱导性多潜能干细胞有着重要的临床应用价值,因此将诱导性多潜能干细胞用于临床治疗前,需要严格分析它的安全性。最早Yamanaka实验小组筛选出的4个多能性基因中[1],c-Myc是一种原癌基因,且Klf4也有一定的致癌性。为了提高诱导性多潜能干细胞的安全性,科学家们做了很多研究。
2009年,斯坦福大学研究者Sun等[11]发现,脂肪干细胞比皮肤成纤维细胞更容易被诱导为诱导性多潜能干细胞,且产生的诱导性多潜能干细胞安全性也更高。Hong等[9]证实在p53缺失的情况下,可以将终末分化的T淋巴细胞去分化而重编程为诱导性多潜能干细胞;且DNA芯片的分析结果发现:在小鼠和人的成纤维细胞中有34个与p53调节有关的基因,对这些基因的功能分析表明,阻断p53-p21通路不仅提高了诱导性多潜能干细胞的转化效率,也降低了诱导性多潜能干细胞的致癌性。但是,如果持久抑制p53反而会增强基因组的不稳定性从而影响诱导性多潜能干细胞的生成。
此外,还有研究小组通过Cre/LoxP重组酶系统来去除诱导性多潜能干细胞中的外源重编程因子从而得到无外源因子的诱导性多潜能干细胞[2],但此方法的缺陷是Cre/LoxP重组酶系统介导的外源因子去除后,载体序列还留在插入位点上,所以仍然无法避免插入突变。而之后Kaji等[22]通过应用PiggyBac转座子传递系统清除融合到宿主基因组中的转基因序列,从而获得了没有病毒载体整合的诱导性多潜能干细胞。
Zhou等[23]则通过短肽介导的蛋白转导的方法将Oct4、Klf4、Sox2、c-Myc这4种蛋白转入小鼠胚胎成纤维细胞和人新生胎儿成纤维细胞也成功得到了诱导性多潜能干细胞。从反转录病毒转染到Cre/LoxP重组酶系统再到游离载体以至到重组蛋白,转录因子对供体细胞基因组的影响越来越小,这意味着,研究者得到的诱导性多潜能干细胞越来越自然也越来越安全,这些成果都预示着,通过研究者的努力,诱导性多潜能干细胞在不断迈向临床。
2.2.4 诱导性多潜能干细胞的应用前景与展望 由于诱导性多潜能干细胞与胚胎干细胞的生物学特性非常相似,且不涉及伦理道德问题,因此具有较高的应用价值。诱导性多潜能干细胞可用于分化和移植,还可以建立疾病模型、研究疾病的发病机制、新药物的筛选以及开发出新的治疗方法。
诱导性多潜能干细胞用于建立疾病模型:疾病模型是人们研究疾病发生机制和病理过程的重要基础,但一些人类疾病并不能完全找到细胞或者实验动物模型,诱导性多潜能干细胞的建立可弥补这一缺陷。而体外疾病模型的建立有利于从细胞水平研究疾病的发病机制,进一步也可用于测试新药的毒性和疗效的观察。
2008年,哈弗大学George Daley实验室利用诱导细胞重编程技术把采自10种不同遗传病患者皮肤细胞转变为诱导性多潜能干细胞[24]。
Thomson等(2009)将脊髓性肌萎缩症患者皮肤细胞诱导成的诱导性多潜能干细胞具有脊髓性肌萎缩症特有的基因型,这项研究首次证实了诱导性多潜能干细胞可用于建立疾病模型用于发病机制的研究和治疗药物筛选。
Studer等首次在体外重现用患者神经细胞诱导成的诱导性多潜能干细胞从发育到死亡的整个过程[25]。
2013年,Peng[26]研究者在《国际生物医学研究》杂志上发表,诱导性多潜能干细胞可以在体外分化为男性生殖细胞,这一项研究为治疗不孕不育症提供了一个很好的研究受精卵发育分子机制的模型。
2013年,Moad等[27]利用人的前列腺细胞和膀胱细胞重编程为诱导性多潜能干细胞,建立了疾病细胞模型,这项研究为描述调控前列腺及膀胱分化和发展的机制提供了一个新模型,同时也为转化组织工程中的再生膀胱研究提供了一个不可多得的发展机会。
此外,研究者们还用诱导性多潜能干细胞建立了其他疾病模型,如范可尼贫血症,β地中海贫血症以及家族性自主神经功能障碍症等。总体来看,相比于诱导性多潜能干细胞用于临床治疗的不确定性,在建立疾病模型、研究发病机制和新药筛选方面可能具有更好的优势。
诱导性多潜能干细胞应用于疾病的治疗及治疗新方法的探索:2007年12月,Hanna等[28]用诱导性多潜能干细胞成功治疗了小鼠的镰状红细胞贫血症。
2009年初,Xu等[29]用从诱导性多潜能干细胞诱导来的内皮前体细胞和内皮细胞成功治疗血友病A。
2009年8月,利用诱导性多潜能干细胞治疗罕见疾病也开始露出曙光,美国斯隆-凯特林研究所的Lee等[30]研究人员首次用诱导性多潜能干细胞建立了家族性植物神经功能不全症的细胞模型。这些成果验证了诱导性多潜能干细胞在基因治疗中的可行性,从理论和实践上为人类单基因遗传病治疗奠定了基础。
2012年,Song等[31]首次报道:人类肾小球系膜细胞重新编程而来的诱导性多潜能干细胞经生肾因子RA、activin-A和骨形态发生蛋白7诱导10 d后便具有了肾小球足细胞的特征,如WT-1、Nephrin、突触蛋白的表达上调;去除生肾因子后,该诱导性多潜能干细胞来源的足细胞仍然具有增殖活性,并且证实这些足细胞具有摄取蛋白的功能及对血管紧张素Ⅱ的反应性。该项研究在一定程度上解决了之前关于肾小球诱导分化困难的问题。
Tatsuy Yoshikawa等[32]研究者报道,系统性应用丙戊酸和唑尼沙胺可以促进诱导性多潜能干细胞分化为多巴胺能神经元细胞,此项研究可以应用于治疗帕金森疾病的黑质纹状体多巴胺能神经元的缺失,为一些神经系统功能性损伤及缺失的疾病带来希望。
总的来说,在诱导性多潜能干细胞的应用中,可以通过生长因子诱导、与其他细胞共培养或形成类胚体的途经诱导正常人和患者诱导性多潜能干细胞定向分化。比较正常和疾病来源的诱导性多潜能干细胞在正常或各种刺激条件下生长、分化、凋亡、附着、运动及细胞特有功能的不同,建立研究疾病的细胞模型。还可以利用这些细胞模型运用各种组学技术,分析正常细胞和疾病细胞之间的细胞编程差异。另外,根据每一种重大疾病中涉及到的基因产物不同,通过不同的生物化学、分子生物学、细胞生物学和物理学等手段进一步研究疾病发生的分子机制,这些分子机制的研究有助于研究者们发现疾病治疗的新靶点并寻找到针对性的新药物和治疗方法,还可以利用建立的疾病细胞模型来检验新药,筛选出对特异靶点或者细胞表型有影响的药物或治疗方法,也有望实现对某些重大疾病的有效治疗甚至实现个体化治疗。
